23.依據醫療器材查驗登記審查準則之規定,進行臨床前測試檢測之受託實驗室,執行下列何項試驗,不須符合
ISO/IEC 17025或藥物非臨床試驗優良操作規範(GLP)之規定?
(A)機械力學
(B)電性安全性
(C)生物相容性
(D)無菌性試驗
答案:登入後查看
統計: A(2786), B(411), C(370), D(355), E(0) #2865231
統計: A(2786), B(411), C(370), D(355), E(0) #2865231
詳解 (共 7 筆)
#6149517
生物相容性、電性安全性、電磁相容性檢測及無菌性試驗
ㅤㅤ
口訣:GLP電電無聲
ㅤㅤ
ㅤㅤ
ㅤㅤ
只有(A) 機械力學 沒性
33
0
#5714602
補充一下 醫材相關條文的廢止
| 廢止 111.03.16起 |
改用 |
| 醫療器材查驗登記審查準則 | 醫療器材許可證核發與登錄及年度申報準則 |
| 醫療器材管理辦法 | 醫療器材分類分級管理辦法 |
| 醫療器材查驗登記及廣告審查費收費標準 | 醫療器材行政規費收費標準 |
以上於110.09.30 公告 (來源)
31
3
#5854920
醫療器材許可證核發與登錄及年度申報準則(發布日期:民國 110 年 04 月 29 日)
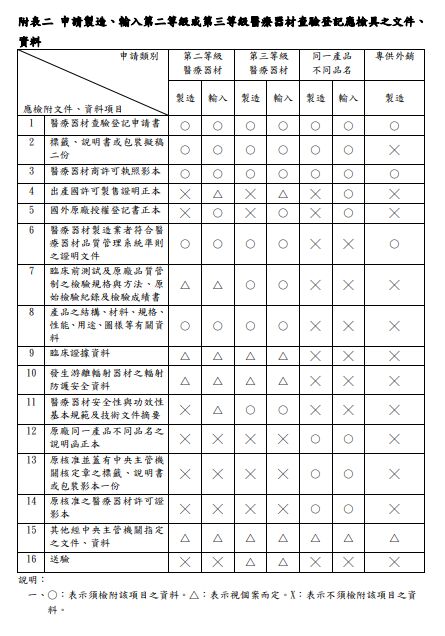
附表二 申請製造、輸入第二等級或第三等級醫療器材查驗登記應檢具之文件、資料
七、臨床前測試及原廠品質管制之檢驗規格與方法、原始檢驗紀錄及檢驗成績書:
(一) 本項文件包括為確保產品宣稱效能、結構、材質、設計及品質所進行之安全性
及功能性檢測等資料。
(二) 已有類似品經中央主管機關核准上市之第二等級醫療器材者,得以下列文件之
一替代之:
1、 與我國訂有醫療器材上市前審查技術合作協議國家官方所出具之核准上市證
明文件,以及醫療器材安全性與功效性基本規範及技術文件摘要。
2、 中央主管機關公告之品項,且製造業者曾有相同分類分級品項之類似品經中
央主管機關核准上市者之醫療器材臨床前測試資料切結書。
(三)附表三之第二等級醫療器材,同一製造業者有同一品項之類似品經中央主管機關
核准上市,且該許可證仍於有效期限者,得以有類似品之第二等級醫療器材產品
比較暨臨床前測試資料符合性聲明書替代之。
(四) 經中央主管機關公告應辦理檢驗之醫療器材者,本項文件應檢附二份。
(五) 執行檢測生物相容性、電性安全性、電磁相容性檢測及無菌性試驗之受託實驗
室,應符合下列條件之一:
1、 符合 ISO/IEC 17025 之規定。
2、 符合非臨床試驗優良操作規範(GLP)之規定。
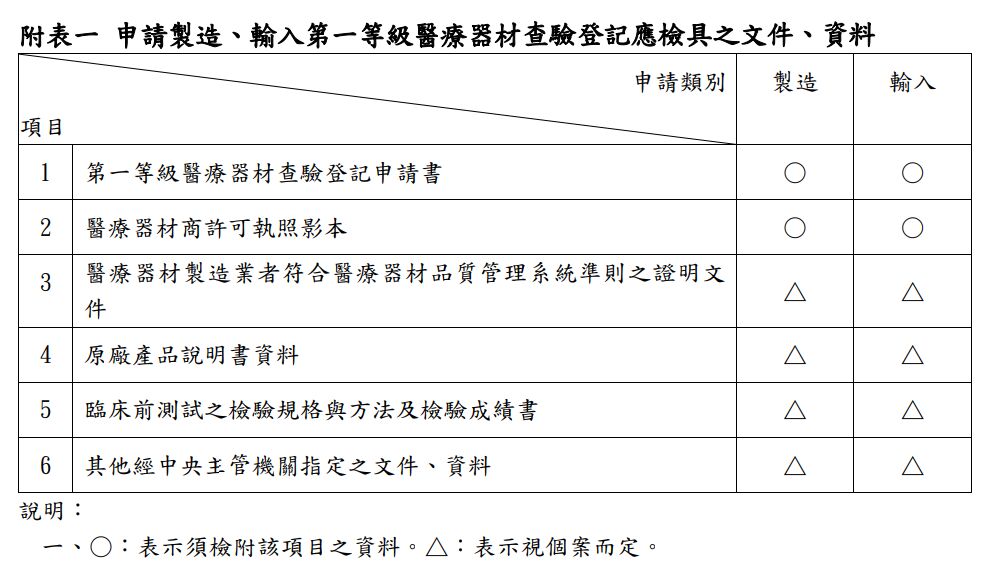
另外,申請第一等級與二、三等級醫材查驗登記應檢具之文件、資料不太一樣
17
5