4. 某金屬結構為面心立方單位晶格,晶格邊長為360 pm,該金屬的密度為8.96 g/cm3
,請問該金
屬最可能為下列何者?
(A) Cu(63.5)
(B) Ag(108)
(C) Au(197)
(D) Cs(133)
答案:登入後查看
統計: A(56), B(2), C(3), D(6), E(0) #2799546
統計: A(56), B(2), C(3), D(6), E(0) #2799546
詳解 (共 2 筆)
#5688356
面心立方單位晶格含有4個原子,設金屬分子量為X g/mole
1 pm=10-10 cm
密度=質量/體積 = 4*X / 6.02*1023 (g) / (360*10-10)3 (cm3) = 8.96
得X ≒ 63.5
1 pm=10-10 cm
密度=質量/體積 = 4*X / 6.02*1023 (g) / (360*10-10)3 (cm3) = 8.96
得X ≒ 63.5
1
0
#7291802
面心立方晶格如下圖,而面心立方的單位晶格含有4個原子,假設金屬分子量為X g/mole。其中1 pm = 10-12 m = 10-10 cm。
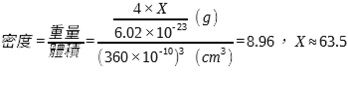 答案(A)
答案(A)
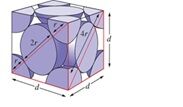 Chemical Principles by Steven S. Zumdahl, Donald J. DeCoste8th,666
Chemical Principles by Steven S. Zumdahl, Donald J. DeCoste8th,666
0
0