28.依據藥品查驗登記審查準則,關於原料藥申請案之敘述,下列何者錯誤?
(A)製劑申請新增或變更原料藥來源,若依劑型特性之製劑成品檢驗結果比對評估不一致者,應立即駁回其申 請
(B)原料藥指一種經物理、化學處理或生物技術過程製造所得具藥理作用之活性物或成分,常用於藥品、生物 藥品或生物技術產品之製造
(C)外銷專用之製劑及原料藥查驗登記申請案,除經中央衛生主管機關認有必要送驗者外,得以書面審核而免 送驗樣品
(D)原料藥查驗登記檢送資料應以通用技術文件格式呈現
答案:登入後查看
統計: A(2121), B(196), C(1035), D(171), E(0) #3197596
統計: A(2121), B(196), C(1035), D(171), E(0) #3197596
詳解 (共 5 筆)
#6106380
(A)簡單來說就是需要另檢送藥品生體相等性試驗報告,如果還是不通過才會被駁回申請
142
1
#6073946
題解
ㅤㅤ
28.依據藥品查驗登記審查準則,關於原料藥申請案之敘述,下列何者錯誤?
ㅤㅤ
(A) 製劑申請新增或變更原料藥來源,若依劑型特性之製劑成品檢驗結果比對評估不一致者,應立即駁回其申請
ㅤㅤ
→藥品查驗登記審查準則 第 49-1 條
已領有許可證之原料藥及製劑之原料藥,其技術性資料變更應檢附資料如附件十二。
申請製劑新增或變更原料藥來源,應檢附下列資料:
一、藥品變更登記申請書。
二、藥品許可證正本。
三、新增或變更之有效成分符合藥品優良製造規範證明文件。
四、該原料藥技術性資料經中央衛生主管機關核准之證明文件。但經中央衛生主管機關公告得以其他資料替代之藥品,不在此限。
五、新舊有效成分規格差異之說明及其佐證。
六、依劑型特性之製劑成品檢驗結果比對評估資料。
七、前款比對評估不一致者,應執行溶離率曲線比對,若比對結果不相似者(f2<50),應另檢送藥品生體相等性試驗報告。
ㅤㅤ
(B) 原料藥指一種經物理、化學處理或生物技術過程製造所得具藥理作用之活性物或成分,常用於藥品、生物 藥品或生物技術產品之製造
ㅤㅤ
→藥品查驗登記審查準則第 4 條
ㅤㅤ
本章用詞定義如下:
一、新藥:指本法第七條所稱之新藥。
二、學名藥:指與國內已核准之藥品具同成分、同劑型、同劑量、同療效之製劑。
三、生物藥品:指依據微生物學、免疫學學理製造之血清、抗毒素、疫苗、類毒素及菌液等。
四、原料藥(藥品有效成分):指一種經物理、化學處理或生物技術過程製造所得具藥理作用之活性物或成分,常用於藥品、生物藥品或生物技術產品之製造。
五、核醫放射性藥品:指符合本法第六條所稱藥品之定義,並係以具有放射活度之物質使用於人體內,經體內分佈之後,可被用來診斷、監測、治療、緩解疾病或具其他醫療效能之藥品。
ㅤㅤ
(C) 外銷專用之製劑及原料藥查驗登記申請案,除經中央衛生主管機關認有必要送驗者外,得以書面審核而免 送驗樣品
ㅤㅤ
→藥品查驗登記審查準則第 24 條
ㅤㅤ
本章規定之各類申請案件,除別有規定外,其審查以書面審核與藥品送驗作業併行。如書面審核通過者,申請人即應依中央衛生主管機關通知辦理領證手續;如檢驗規格審核通過者,申請人即應依中央衛生主管機關通知辦理送驗手續。
下列申請案,除經中央衛生主管機關認有必要送驗者外,得以書面審核而免送驗樣品:
一、查驗登記:
(一)列屬成藥(含乙類成藥)之製劑。
(二)符合含維生素產品認定基準表之維生素製劑。
(三)學名藥。
(四)新藥。
(五)符合指示藥品審查基準之製劑。
(六)一般原料藥。
(七)外銷專用之製劑及原料藥。
(八)核醫放射性藥品。
(九)過敏原藥品。
二、變更登記。
前項採書面審核之藥品,申請人須加送樣品掃描檔或彩色圖片供審查。必要時,應依中央衛生主管機關通知,提供對照標準品,以利比對。
ㅤㅤ
(D) 原料藥查驗登記檢送資料應以通用技術文件格式呈現
ㅤㅤ
→藥品查驗登記審查準則 附件8
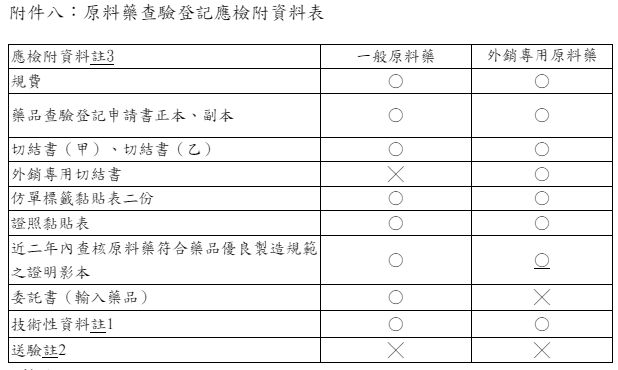
註:
○ 表示須檢附該項目之資料。
△ 表示視個案而定。
╳ 表示不須檢附該項目之資料。
1.參見「原料藥查驗登記應檢附之技術性資料表」。
2.依第二十四條第二項規定,除經中央衛生主管機關認有必要送驗者外,
得以書面審核而免送驗樣品。
3.檢送資料應以通用技術文件(Common Technical Document,CTD)格式呈現。
○ 表示須檢附該項目之資料。
△ 表示視個案而定。
╳ 表示不須檢附該項目之資料。
1.參見「原料藥查驗登記應檢附之技術性資料表」。
2.依第二十四條第二項規定,除經中央衛生主管機關認有必要送驗者外,
得以書面審核而免送驗樣品。
3.檢送資料應以通用技術文件(Common Technical Document,CTD)格式呈現。
102
1