34.某新成分新藥於104年3月1日於日本首度上市,由藥廠甲於107年2月1日申請查驗登記,於108年10月1日核准
取得新成分新藥許可證。藥廠乙欲提出該新藥成分之學名藥申請時,可於何時提出申請?何時可領到衛生福
利部核發之學名藥許可證?
(A)107年3月1日後;109年3月1日後
(B)110年2月1日後;112年10月1日後
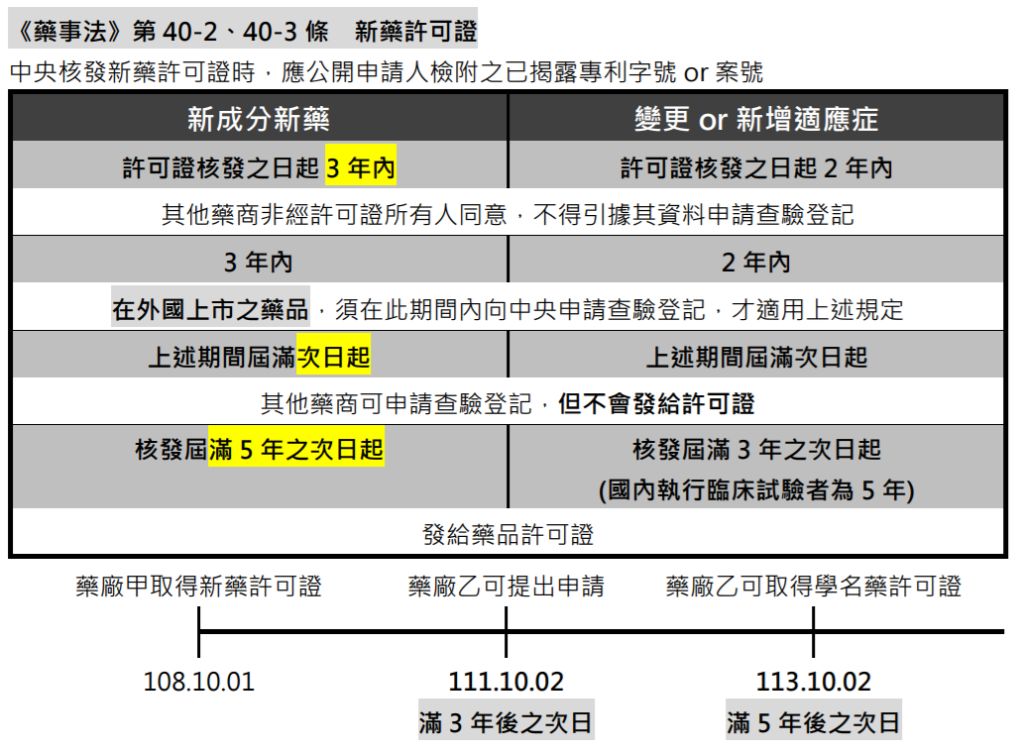
(C)111年10月1日後;113年10月1日後
(D)108年10月1日後;無時間限制
統計: A(326), B(610), C(5517), D(153), E(0) #2180318
詳解 (共 10 筆)
樓上好像沒複製到關鍵句...補個
4.某藥品 A 於西元 2000 年在美國上市外,皆未於其他國申請查驗登記,2008 年 2 月 2 日由我國代理商甲申請查驗登記,於 2009 年 8 月 8 日取得許可證。某藥廠乙於 2009 年 5 月 5 日以同成分、同劑型、同劑量及同單位含量藥品申請查驗登記,衛生主管機關於 2010 年 8 月 8 日審查通過,則下列敘述何者正確?
(A) 我國代理商甲依藥事法第 40 條之 2 之規定享有資料專屬權(Data Exclusivity)
(B) 藥廠乙無須取得代理商甲之同意,即得引據藥品 A 之資料申請查驗登記
(C) 衛生主管機關於 2014 年 5 月 5 日以前不得核給許可證
(D) 藥廠乙應於 2011 年 2 月 2 日以後方准申請查驗登記 .
個人: 尚未作答
想請問,藥事法第40-2條
其中甲因為3年內申請新藥許可證,所以符合該條第四項的要件,因此適用該條第二項,但是並沒有說到適用第三項之規定。
我在想這樣藥廠乙是不是應該111年10月1日後就可以拿到藥證?
(更新,謝謝8F的回答,了解了,謝謝你)
附上條文
----------
第40-2條
第一項、中央衛生主管機關於核發新藥許可證時,應公開申請人檢附之已揭露專利字號或案號。
第二項、新成分新藥許可證自核發之日起三年內,其他藥商非經許可證所有人同意,不得引據其申請資料申請查驗登記。(適用)
第三項、前項期間屆滿次日起,其他藥商得依本法及相關法規申請查驗登記,符合規定者,中央衛生主管機關於前項新成分新藥許可證核發屆滿五年之次日起,始得發給藥品許可證。(沒有說適用)
第四項、新成分新藥在外國取得上市許可後三年內,向中央衛生主管機關申請查驗登記,始得適用第二項之規定。(藥廠甲滿足此要求)
| 學名藥廠可申請 | 學名藥廠可領證 | |
| 新成分新藥 | 1.許可證核發日起3年 2.在外國取得上市許可的3年內 |
1.許可證核發日起5年 |
| 新增或變更適應症 | 1.中央核准新增或變更日起2年 2.在外國取得上市許可的2年內 |
1.中央核准新增或變更日起3年 2.於國內執行臨床試驗:中央核准日起5年 |
簡易版
| 可申請 | 可領證 | |
| 新成分新藥 | 3 (國外:3 |
5 |
| 新增變更適應症 | 2 (國外:2 |
3 (國內試驗:3 |
To 7F
應該說,第三項本來就是在先有了第二項的大前提下進行規範,只是把最快能查驗登記的時間點,和最快能拿到藥證的時間點分項敘述而已。符合第二項資格,自然就有第三項的保護。
有點不好意思,不太清楚你所謂的「適用」與否指的是怎樣的條件呢?><
個人淺見,有錯請指教
想請問各位大大
藥廠甲107年2月1日申請查驗登記,為什麼108年10月就可以拿到許可證了?
不是要等5年才拿的到嗎@@