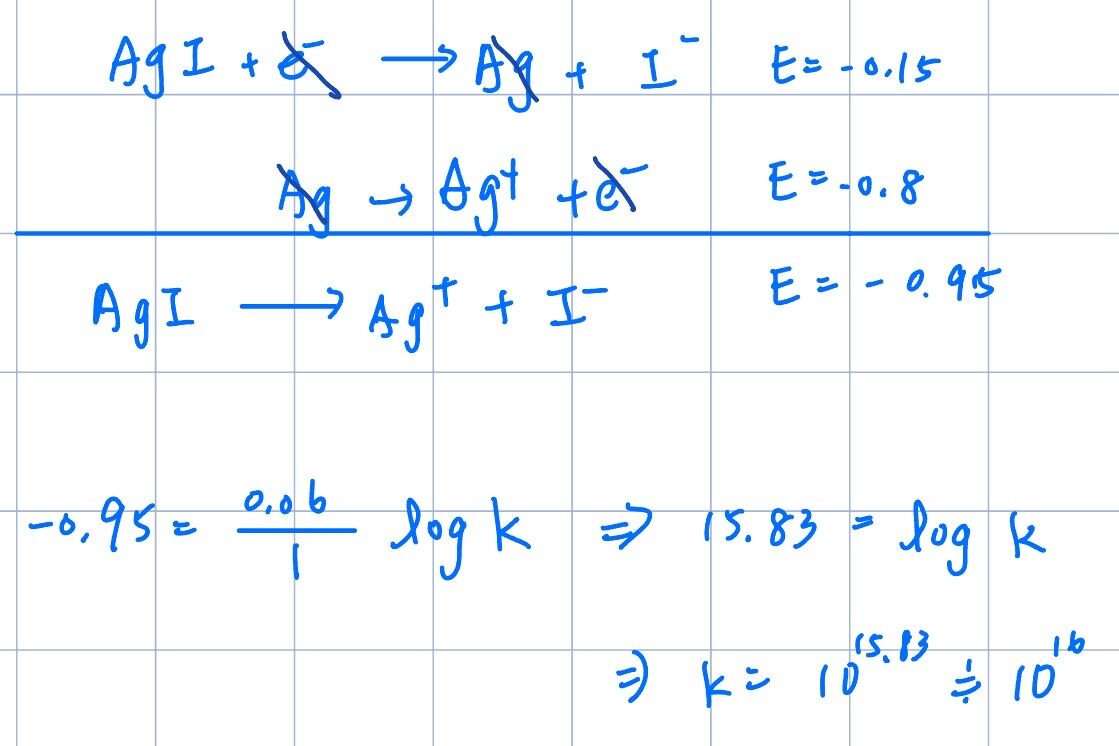9. 使用下列的半反應電位,25 °C 下碘化銀(AgI)的溶解度積(solubility product)為何? 
(A)2.9 x 10–3
(B) 1.9 x 10–4
(C) 2.1 x 10–12
(D) 9.0 x 10–17
(E) 2.4 x 10–20
答案:登入後查看
統計: A(24), B(47), C(53), D(367), E(22) #1992566
統計: A(24), B(47), C(53), D(367), E(22) #1992566
詳解 (共 6 筆)
#3732406
Hint:熟記自由能、電位、平衡常數三者互相轉換的公式
這裡使用電位與平衡常數的轉換公式,E=(RT/nF)lnK
又因為在25°C,E=(0.0592/n)logK
從題目要求的反應方程式求出E=-0.15-0.8=-0.95V
代入公式,-0.95=(0.0592/1)logK,logK=-16點多
故K為某某數x10-17(有選項的時候可以從選項找答案,不必細算)
答案選(D)
40
1
#6341999
免費公開
Hint:熟記自由能、電位、平衡常數三者互相轉換的公式
這裡使用電位與平衡常數的轉換公式,E=(RT/nF)lnK
又因為在25°C,E=(0.0592/n)logK
從題目要求的反應方程式求出E=-0.15-0.8=-0.95V
代入公式,-0.95=(0.0592/1)logK,logK=-16點多
故K為某某數x10-17(有選項的時候可以從選項找答案,不必細算)
答案選(D)
ㅤㅤ
ㅤㅤ
ㅤㅤ
看題目
詳解卡解鎖
E=-0.15-0.8=-0.95
E=(-RT/n)lnK=(0.059/1)logK=8.17*10^-17
ㅤㅤ
ㅤㅤ
ㅤㅤ
看題目
免費公開
平衡狀態下 E0=0.0592/n x logK阿 所以題目給E0
而且你第一個公式打錯了 是
E=E0- 0.0592/n x logQ 不是K
ㅤㅤ
ㅤㅤ
0
1
#3487459
E=Eo-(0.059/1)logK
為什麼 這題不是 E = -0.95 -(0.059/1)logK 呢? 雖然沒答案
題目給的 不是指 Eo嗎
0
1